Farmakologien er senest opdateret december 2024 og opdateres ikke mere. Siderne lukkes ned til juli 2025.
Indhold
Fordeling
Efter absorptionen fordeles lægemidlet over større eller mindre dele af organismen. Fordelingen omfatter alle de processer, der medvirker til lægemidlets udbredelse i organismen.
1. Fordeling med blodet
For at et lægemiddel kan komme fra absorptionsstedet til blodbanen, må stoffet passere en række cellemembraner, fx i tarmslimhinde, bindevæv og blodkapillærer.
Det samme gælder, når lægemidlet skal fordeles i organismen. Her skal det passere kapillærmembranen, dvs den membran der adskiller blodet og vævsvæsken, for at komme hen til virkningsstedet. Endvidere skal lægemiddelstoffet i forbindelse med eliminationen passere membraner i nyrerne.
2. Stofudveksling
Når lægemidlet har udøvet sin virkning, skal det udskilles og må træde ind i blodbanen igen for at blive transporteret til udskillelsesorganerne. Fig. 7 illustrerer den stofudveksling, der til stadighed foregår mellem blod og væv.
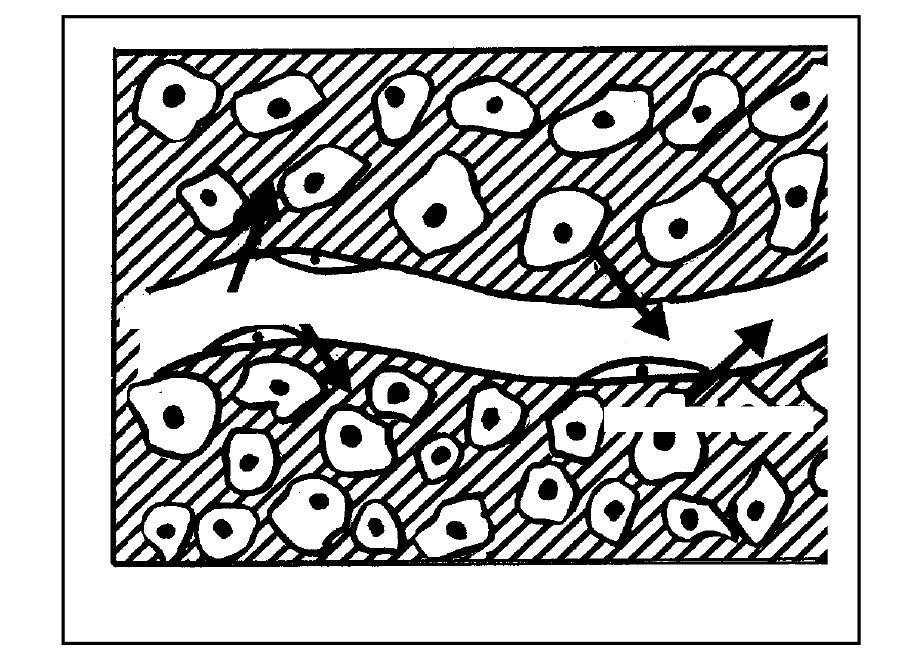
Fig.7: Stofudveksling mellem blod og væv
Idet den primære fordeling sker med det cirkulerende blod, er blodgennemstrømningen i de enkelte væv og organer af afgørende betydning for den hastighed, hvormed lægemidlet når det enkelte væv eller organ.
Blodgennemstrømningen er fx stor i hjerte, hjerne, lunger og nyrer. Koncentrationen og virkningen af et lægemiddel bliver derfor hurtigt større her end i væv og organer med en lille blodgennemstrømning. Det gælder fx fedt‑ og knoglevæv.
Faktorer som påvirker fordelingen
Efter fordelingen med det cirkulerende blod vil lægemidlet i varierende grad optages i forskellige væv og organer. Langt de fleste lægemidler fordeler sig ikke ligeligt i hele organismen. Flere faktorer har indflydelse på denne fordeling. Det gælder:
- Lægemidlets opløselighedsforhold
- Binding til plasmaproteiner
- Egenskaber ved forskellige membraner
- Binding til væv og organer
1. Lægemidlets opløselighedsforhold
Passagen af lægemiddelstof gennem cellemembranen ud til virkningsstederne kræver bl.a., at stofferne er både vand‑ og lipidopløselige.
Stoffer, der er lipidopløselige, vil lettere passere de lipidholdige cellemembraner, fx kapillærmembranen. Samtidig er det dog nødvendigt, at stofferne også er vandopløselige, da transporten med blodet foregår opløst i blodplasma.
2. Binding til plasmaproteiner
Plasmaproteinbinding
De fleste lægemidler bindes i større eller mindre grad til proteiner i blodet. Hyppigst sker bindingen til albumin, der fungerer som transportør for lægemiddelstoffet. Proteinbindingen medfører en skæv fordeling af lægemidlet i organismen, idet plasmaproteiner er for store til at kunne passere cellemembranen, og lægemidlet således forbliver i blodet.
Lægemidlerne bindes til bestemte bindingssteder, kaldet „sites‟ på albuminet. Det medfører, at lægemidlerne i blodet optræder både på en fri og en proteinbundet form på samme tidspunkt (fig. 8).
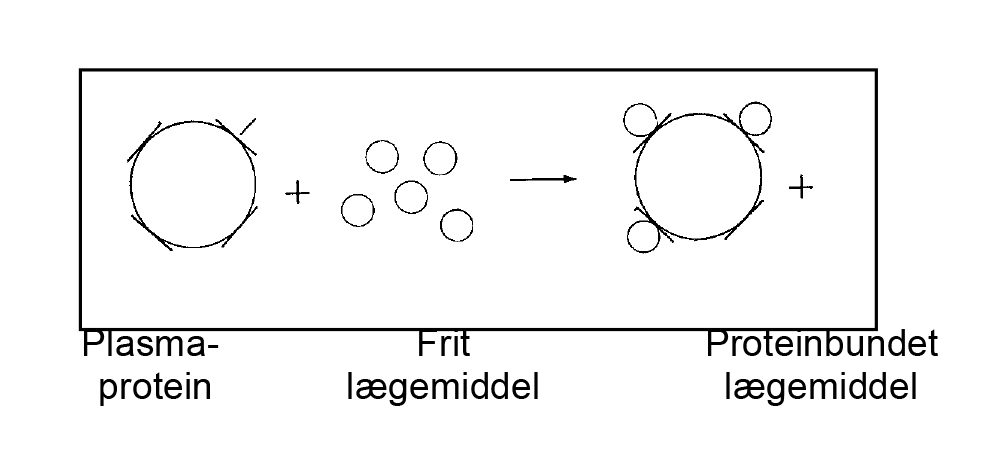
Fig.8: Plasmaproteinbinding
Grad af proteinbinding
Graden af proteinbinding er forskellig fra lægemiddel til lægemiddel og varierer fra 0% ‑ 99%. Endvidere ses individuelle variationer, idet det samme lægemiddel, indgivet til flere personer, bindes i forskellig grad, afhængig af bl.a. albuminkoncentrationen i blodet.
Frit lægemiddel
Den vigtigste konsekvens af plasmaproteinbindingen er lægemidlets ændrede fordeling i organismen. Det skyldes, at kun det frie lægemiddel er i stand til at passere cellemembraner, fx kapillærmembranen, og nå de væv eller organer, hvor det skal udøve en farmakologisk effekt. Det er også kun det frie lægemiddel, der kan udskilles i nyrerne ved glomerulær filtration.
Ligevægt
Efterhånden som den frie del af lægemidlet passerer fra blodet ud i vævene, vil der frigøres mere af den proteinbundne del, idet der hele tiden indstiller sig den samme ligevægt mellem frit og proteinbundet stof i plasma, karakteristisk for hvert enkelt lægemiddelstof. På den måde vil alt lægemiddel efterhånden blive fraspaltet for, dels at kunne udøve en effekt, dels blive udskilt af organismen.
Depoteffekt
Det proteinbundne lægemiddel fungerer herved som et depot, hvorfra frit lægemiddelstof afgives. Stoffer med høj proteinbindingsgrad udskilles dog ikke altid langsomt af organismen, idet styrken af proteinbindingen spiller en afgørende rolle. Visse penicilliner har fx en høj proteinbindingsgrad (over 95%) men udskilles hurtigt, fordi bindingen til plasmaproteinerne er relativt „ løs‟.
3. Egenskaber ved forskellige membraner
Nogle membraner udgør en betydelig passagehindring for lægemidlers fordeling i organismen, idet de ikke eller kun i begrænset omfang tillader lægemidler at passere igennem.
Blod-hjernebarrieren
Blod‑hjernebarrieren er et eksempel på denne type membran. Den består af et ekstra cellelag i de kapillærer, der omgiver centralnervesystemet, og hvorigennem lægemiddelstoffer udveksles til centralnervesystemet. Blod-hjernebarrieren beskytter herved nervevævet mod indtrængen af fremmede stoffer, bl.a. visse lægemidler.
Forudsætningen for passage af denne membran er, at stofferne er udtalt lipidopløselige og har en ringe proteinbinding. I modsætning hertil vil vandopløselige og stærkt proteinbundne stoffer kun vanskeligt kunne passere blod‑hjernebarrieren.
Lægemidler, der skal udøve deres virkning inden for centralnervesystemet, skal derved have en høj grad af lipidopløselighed. Det gælder fx psykofarmaka og sovemidler.
Mange antibiotika, fx penicilliner, holdes normalt effektivt ude fra centralnervesystemet. Det er hensigtsmæssigt, da de har vist sig at være toksiske, hvis de injiceres intrathekalt (inden for kraniet). Penicilliner kan dog anvendes til behandling af meningitis, hvor blod-hjernebarrieren er betændt. Her er passagen af penicillin ind i centralnervesystemet nogenlunde god.
Placentamembran
Placentamembranen er den membran, der adskiller fosterets blod fra moderens. Gennem membranen passerer næringsstoffer fra moderens blod til fosteret.
Placentamembranen er mere gennemtrængelig for stoffer end blod‑hjernebarrieren og hindrer derfor ikke fuldstændigt passage af lægemidler til fosteret. Fordelingen af lægemidler til fosteret er dog forsinket i forhold til moderen, og det tager længere tid, inden fosterblodet opnår samme lægemiddelkoncentration som moderens blod.
Passage af lægemidler gennem placentamembranen medfører, at fosteret kan påvirkes og evt. skades.
Disse forhold er uddybet i afsnittet Lægemidler og graviditet.
4. Binding til væv og organer
Lægemidler kan bindes til bestemte væv eller organer, hvilket medfører en skæv fordeling. Eksempler er diazepam og midazolam, der bindes til fedtvæv. Et andet eksempel er tetracyclin, der bindes til knogle‑ og tandvæv, hvor det kan forblive i mange år efter indgiften.
Omfordeling
Bindingen af et lægemiddel sker ofte i forbindelse med en omfordeling, hvor lægemidlet bindes og transporteres fra et væv til et andet. Under en omfordeling ophører lægemidlet med at virke, idet lægemidlet bindes til et andet væv end virkningsstedet. Ophør i virkning skyldes ellers normalt, at lægemidlet omdannes til inaktive forbindelser eller udskilles af organismen.
Et eksempel på en omfordeling ses ved nogle lægemidler til i.v. anæstesi, fx thiopental (fig. 9). 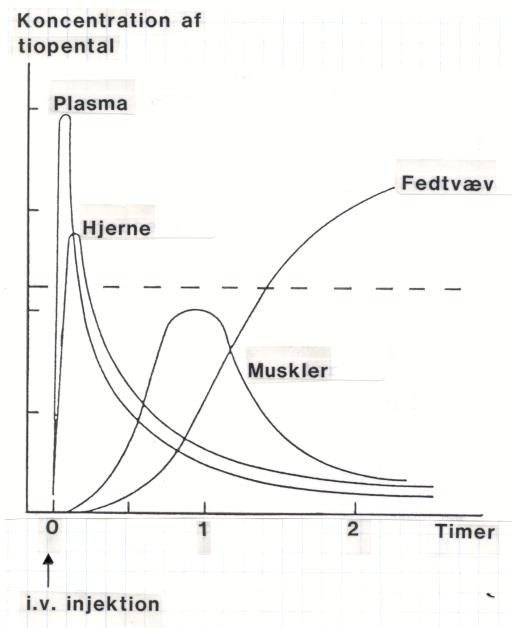
Fig.9: Omfordeling af thiopental
Efter indgift af thiopental opnås hurtigt høje koncentrationer i hjernen på grund af centralnervesystemets store blodgennemstrømning, hvorved fuld bedøvelse opnås. Den bedøvende virkning af thiopental aftager dog hurtigt. Det skyldes, at stoffet i løbet af kort tid transporteres fra centralnervesystemet til muskel‑ og fedtvævet. Her bindes det, og i fedtvævet kan stoffet forblive i lang tid. Thiopental udgør her et depot, hvorfra det langsomt udskilles. Patienten er ikke længere bedøvet, men har altså stadig stoffet i kroppen.
