Farmakologien er senest opdateret december 2024 og opdateres ikke mere. Siderne lukkes ned til oktober 2025.
Indhold
Placentapassage og fosterets farmakologi
- Transporten via placentamembranen
- Fysisk-kemiske egenskaber ved lægemidlet
- Specielle farmakokinetiske forhold hos moderen og fosteret
- Medikamentel terapi af fosteret
Placentapassage og fosterets farmakologi
Hvorvidt et lægemiddel, som gives til moderen, kan virke på fosteret, er i sidste instans afhængig af, i hvilken grad lægemidlet passerer placentamembranen. Langt de fleste lægemidler har sådanne egenskaber, at en del af den indtagne dosis når frem til fosteret. På den anden side er placentapassage absolut ikke ensbetydende med, at stoffet dermed kan fremkalde fosterskader. Der kendes mange eksempler på lægemidler, der meget let passerer placenta, men som ikke har nogen beviselig fosterskade.
Placentapassagen afhænger af farmakokinetiske egenskaber ved lægemidlet. I det følgende gives en oversigt over de vigtigste faktorer, som er bestemmende for placentapassagen af lægemidler.
1. Transporten via placentamembranen
Passage af lægemidler gennem placenta er næsten udelukkende passiv, dvs. diffusion følgende de almindelige regler for lægemidlers passage af biomembraner.
Placenta er mere gennemtrængelig end mange andre af organismens membraner og slet ikke så selektiv som fx blod-hjernebarrieren. især tillader placenta i højere grad end blod-hjernebarrieren passage af vandopløselige stoffer.
Specialiseret transport spiller derimod en stor rolle for transporten af biologiske stoffer som aminosyrer, glukose, vandopløselige vitaminer og visse ioner. Hvis moderens indtagelse af kalk og jern er utilstrækkelig til at dække både moderens og barnets behov, er det ofte kun moderen, som kommer til at lide under mangelen. Kun i enkelte tilfælde, hvor den kemiske struktur ligner de biologiske stoffer, har denne transportform betydning for lægemidler. Dette gælder eksempelvis digoxin, visse cytostatika, visse antiepileptika og lægemidler mid HIV-virus.
I nogle tilfælde kan transporten over placenta også foregå ved faciliteret diffusion, pinocytose, fagocytose eller passage via beskadiget membran.
Det kan tage relativt lang tid, inden ligevægt er indstillet. Derfor ses som regel lavere koncentration i fosterets blod end i moderens.
Faktorer, der begunstiger passage af placenta:
- molekylvægt < 600
- udpræget lipidopløselighed
- ringe ionisation
- ringe proteinbinding
- god blodgennemstrømning af placenta
2. Fysisk-kemiske egenskaber ved lægemidlet
Lipidopløselighed og dissociationsgrad
Lægemidler, der er lipidopløselige og primært forekommer i uioniseret tilstand ved den fysiologiske pH, er blandt de stoffer, som hurtigt passerer placenta. Mens polære stoffer, som er stærkt ioniserede ved den fysiologiske pH, synes at passere langsommere.
Proteinbinding
Proteinbindingsgraden er lavere hos fosteret end hos moderen. Et stærkt proteinbundet lægemiddel må således forventes at have lavere totalkoncentration i plasma hos fosteret end hos moderen, når diffusionsligevægt er indtrådt.
På grund af den store forøgelse af plasmavolumenet under graviditeten er albuminkoncentrationen hos moderen ved fødselstidspunktet betydeligt lavere end hos ikke-gravide. Barnet vil altså mod slutningen af graviditeten have relativt større albuminkoncentration end moderen og dermed større proteinbindingskapacitet. Dette betyder, at proteinbindingen for nogle lægemidler mod slutningen af graviditeten er højest hos fosteret. Hos mennesker finder man da også højere salicylatkoncentrationer i plasma hos det nyfødte barn end hos moderen. Det samme gælder fx diazepam, phenobarbital (Fenemal), phenytoin og valproat og visse antibiotika.
Molekylvægt
Store molekyler, fx heparin, thyroxin eller dextran, kan vanskeligt passere placenta. Som en grov regel gælder, at stoffer med en molekylvægt over 1000 ikke passerer. Der findes dog visse store molekyler, som kan passere, fx globuliner. Endog erytrocytter kan i nogle tilfælde passere membranen.
Stoffer med en molekylvægt under 600 kan i regelen passere placenta. De fleste anvendte lægemidler har netop en molekylvægt på 200-400. De mellemliggende, altså stoffer med molekylvægt mellem 600 og 1000, er det vanskeligt at udtale sig om. Digoxin, der har en molekylvægt på 781, kan let passere placenta.
3. Specielle farmakokinetiske forhold hos moderen og fosteret
Det interessante i systemet lægemiddel-moder-foster er dets kontinuerlige forandring under graviditetens forløb. Lægemiddelmolekylet er det samme, moderorganismen til en vis grad også, men fosteret er hele tiden under udvikling.
Svangerskab frembringer forandringer i moderens organisme. Moderens plasmavolumen og extracellulære væske øges. Albuminkoncentrationen i plasma aftager. Hjertets aktivitet er øget, hvilket medfører, at også nyrefunktionen er øget. Man ser da også, at visse lægemidler, der udskilles renalt, hurtigere elimineres under graviditet. Dette gælder fx lamotrigen, ampicillin, gentamycin, cefazolin, digoxin og litium. Det betyder, at dosis af visse lægemidler må øges under graviditet for at opretholde den nødvendige plasmakoncentration, så der sikres en god effekt. Ændringerne vil sædvanligvis tiltage i løbet af graviditeten og nå sit maksimale i 2. eller 3. trimester. Plasmakoncentrationen normaliseres som regel i løbet af 1-2 uger efter fødslen (16).
Leverens enzymaktivitet øges i 1. og 2. trimester for senere at aftage, men hvad dette betyder for lægemiddelmetabolismen er ikke klarlagt. Ved behandling af gravide med phenytoin opnås ofte lavere plasmakoncentration på grund af stoffets hurtigere metabolisme.
Hos gravide med emesis kan oral indtagelse af nødvendig medicin vanskeliggøres. Der kan være vekslende absorption i forbindelse med opkastning og nedsat patientcompliance, hvilket fører til lavere plasmakoncentration af lægemidlet. Man kan forsøge at udskyde indtagelsestidspunktet til senere på døgnet, hvor kvalmen er mindre udtalt.
Under graviditet ses tillige en nedsat gastrointestiel motilitet, der medfører en forlængelse af ventrikeltømningstiden med 30-50%. Dette kan have betydning, hvis der ønskes en hurtigt indsættende virkning. Under fødslen er ventikeltømningen ligeledes nedsat, hvilket gør oral indtagelse uhensigtsmæssig hos en kvinde i fødsel.
Den placentare blodgennemstrømning
Den fraktion af et udpræget lipidopløseligt lægemiddel, som passerer fra moderen til fosteret, synes at være direkte proportional med den maternelle blodgennemstrømning. Gennemstrømningen på den maternelle side er ca. 500 ml/min og på den føtale side ca. 250 ml/min, altså høje værdier.
Placentas anatomi
Den membran, der adskiller moderens blod fra fosterets blod, er i begyndelsen af graviditeten ca. 25 mikrometer tyk, ved slutningen af graviditeten derimod kun 2-4 mikrometer tyk. Data fra forsøg med gnavere viser, at placentapassagen er langsomst i 2. trimester og hurtigst i 1. og 3. trimester. Permeabiliteten af natriumioner og visse antibiotika øges i slutningen af graviditeten.
Elimination hos fosteret
Både placenta og fosterets lever har enzymer, som er i stand til at metabolisere lægemidler. Placentavæv kan under in vitro omstændigheder metabolisere mange lægemidler, idet der er påvist enzymsystemer, som kan indgå i omdannelse af lægemidler. Hvilken klinisk betydning dette kan have, er stadig uklart. Nogle af metabolitterne kan måske i sig selv være fosterbeskadigende. En del stoffer nedbrydes via epoxider, som kan have både mutagen, carcinogen, cytotoksisk og teratogen effekt. I placenta er også påvist et insulinnedbrydende enzym, insulinase, hvilket måske er med til at forklare det øgede insulinbehov hos diabetikere efter 1. trimester.
Fosteret kan anatomisk set kun skille sig af med stoffer ved passage tilbage til moderens blod og til amnionvæsken, da leverens metaboliske kapacitet er ringe.
Hvis lægemidlet ikke metaboliseres af fosteret, eller hvis det metaboliseres til ikke-vandopløselige metabolitter, vil det i regelen passere tilbage i uændret form over placenta.
Hvis derimod lægemidlet metaboliseres til vandopløselige metabolitter, kan disse dårligt transporteres tilbage via placenta. Sådanne metabolitter kan akkumuleres i fosteret eller udskilles i amnionvæsken.
Efter fødslen må barnet udskille tilført lægemiddel væsentligst ved metabolisme i leveren og ekskretion via nyrerne. Det nyfødte barns kapacitet for elimination af lægemidler er meget lavere end voksnes, og en række lægemidler har en betydelig længere halveringstid hos nyfødte.
Selv om lægemiddelpassage af placenta i nogen grad kan forudses ud fra stoffets fysisk-kemiske egenskaber og proteinbindingsgrad, bevirker placentas komplicerede opbygning og ændringerne i løbet af graviditeten, at eksperimentelle undersøgelser, sammenholdt med kliniske erfaringer, er nødvendige for de enkelte lægemidler. Eksperimenter på mennesker kan sædvanligvis kun foretages omkring fødselstidspunktet, hvor navlesnorsblodet er tilgængeligt for analyse. I enkelte tilfælde er der dog udført undersøgelser hos frivillige gravide kvinder, som har besluttet sig for legal abort.
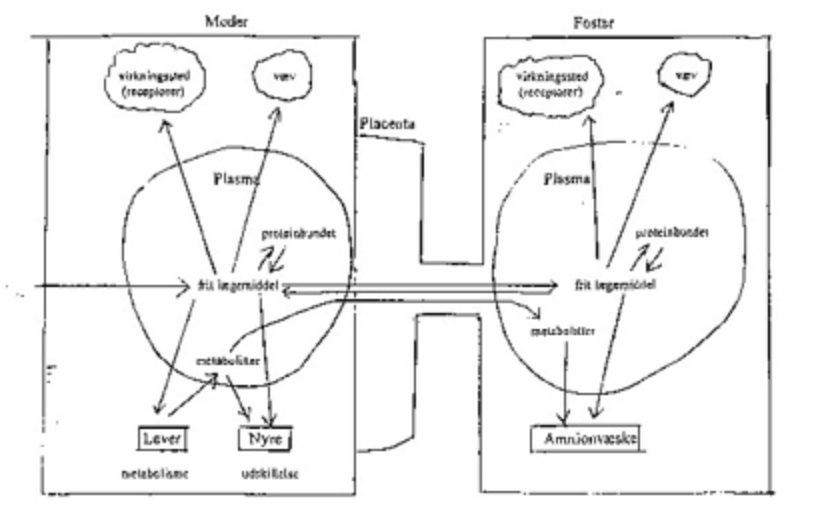
4. Medikamentel terapi af fosteret
Oftest tænker man på risikoen for fosterskader, når lægemidler passserer placentamembranen, men i visse situationer er placentapassage tilstræbt. Dette gælder fx det profylaktiske tilskud af vitaminer, jern og kalk, hvor såvel moder som foster kan nyde gavn af behandlingen. Man kan også opleve situationer, hvor det er fosteret og ikke moderen, der er patient. Det gælder fx glukokortikoider der gives ved truende for tidlig fødsel for at udnytte den modnende effekt på fosterets lungevæv, så respiratorisk distress forebygges.
I nogle tilfælde er det forsøgt at behandle et foster med hjertesygdom. Som eksempel kan nævnes, at intrauterin takykardi er blevet behandlet ved indgift af digoxin til moderen.
Flere antibiotika kan bekæmpe mikroorganismer hos fosteret, samtidig med at moderens infektionssygdom behandles. Dette gælder fx behandling af syfilis med penicillin.
