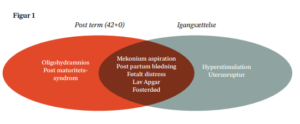
Baggrund: Det er kendt viden, at graviditet, der fortsætter langt ud over estimeret terminsdato, er forbundet med en øget sygelighed hos både den fødende kvinde og hendes barn (1,2). I forbindelse med fødslen er der blandt andet øget risiko for dystoci, post partum blødning og sectio, og for barnet er der øget risiko for blandt andet oligohydramnios, post-maturity syndrome, mekoniumtilblandet fostervand, lav Apgar score og i værste fald død (1). Det er derfor en helt relevant diskussion at tage, om vi kan forbedre maternelle og perinatale udfald ved at sætte fødslerne tidligere i gang. Imidlertid er den behandling, kvinderne tilbydes, ikke risikofri. Det viser sig faktisk, at behandlingen har mange af de samme følgevirkninger, som der findes ved graviditas prolongata (grav.prolong.). Ved igangsættelse er der desuden øget risiko for blandt andet hyperstimulation og uterusruptur.
Figur 1 viser risici og overlap af risici ved hhv. at være grav.prolong. og blive igangsat. En anden vigtig pointe er, at kvinder ikke går spontant i fødsel til en bestemt terminsdato, men med en margin på op til omkring 37 dage (3). Uden indgriben vil den spontant indsættende fødsel altså finde sted over en periode hos langt de fleste kvinder (37+0 til 42+0 gestationsuger). I en normal uforstyrret population vil omkring en fjerdedel stadig være gravide ved 41+0 gestationsuger, mens omkring 4-6% stadig er det, når vi når to uger over termin (42+0 gestationsuger) (4). Det betyder, at hvis igangsættelsen flyttes henimod et tidligere tidspunkt, er der også pludselig mange flere raske gravide kvinder med ukompliceret graviditet, som påføres de risici, som der findes ved en igangsættelse. Vi har illustreret dette i figur 2, der viser, hvor mange kvinder, der fortsat er gravide i ugerne 41 og 42 (to-dages intervaller) (4). Dette giver et indtryk af, hvor mange ekstra igangsættelser en ændret praksis medfører.
Argumentet for at tilbyde tidligere rutinemæssig igangsættelse var primært hensynet til barnet. Da man i 2011 ændrede de danske guidelines, skete det med stor gennemslagskraft, og allerede året efter havde 22 ud af 24 fødesteder indført ændringerne (5). I årene efter ændringen kom der to studier, som viste, at antallet af intrauterine dødsfald var halveret efter praksisændringen (6,7). De offentligt tilgængelige tal fra Sundhedsdatastyrelsen tydede dog nærmere på status quo end en egentlig nedgang i dødeligheden (8). Alligevel indgår resultaterne som vægtige argumenter i offentlige og faglige debatter vedr. anbefalet tidspunkt for igangsættelse efter terminsdatoen (9,10). Der har aldrig været en formel evaluering af denne praksisændring. Formålet med vores studie var derfor at evaluere, hvorvidt den tidligere rutinemæssig igangsættelse medførte nogle fordele såsom fald i dødelighed for barnet, men også om ændringen havde mulige bivirkninger og følgevirkninger.
Metode: Studiet er et registerbaseret kohortestudie. Vi begrænsede populationen til alle graviditeter, der varede til mindst 41+3 gestationsuger (fra 290 dage og fremefter). Vi målte 11 år op til den nye guideline (2000-2010) og 5 år efter (2012-2016). Året 2011 indgik som et overgangsår. Som udgangspunkt er kvinder, der går frem til 41+3 gestationsuger en lavrisikogruppe, idet kvinder med fx IUGR, hypertension, diabetes, højt BMI (>35), høj maternel alder (≥40 år) m.v., har fået deres fødsel sat i gang, inden de når dette tidspunkt.
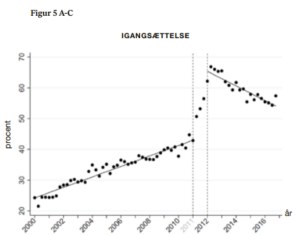
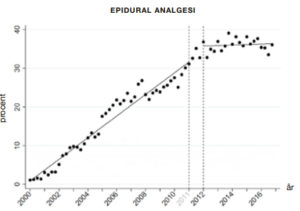
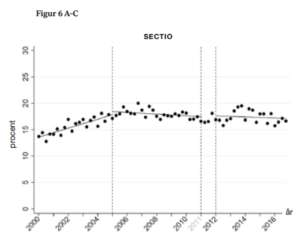
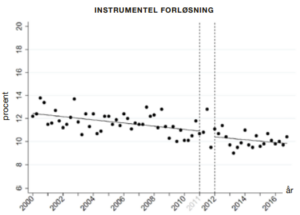
Da det primære argument for den nye igangsættelsespraksis var at redde flere børn fra intrauterin mistrivsel og i værste fald at dø, var vores primære udfald intrauterin fosterdød, perinatal død (intrauterin død eller død inden for første leveuge) og lav Apgar score (<7 efter 5 minutter). Vi var også interesseret i, om der generelt kom flere indgreb ifm. fødslen. Vi undersøgte derfor udviklingen i igangsættelser, epiduralanalgesi og vestimulation og i fødselsudfald som sectio, instrumentel forløsning og uterusruptur.
Studiet opgør ændringer i fødselsrelaterede udfald over tid. Hvis den population, vi undersøger, ændrer sig hen over perioden, kan dette jo være hele eller dele af forklaringen på evt. ændringer i fødselsudfald. Hvis fx kvinderne generelt er blevet mere syge eller mere overvægtige. Derfor undersøgte vi også, om der var sket en ændring over tid med hensyn til andel af førstegangsfødende, kvinder >40 år, tidligere sectio, let- til moderat præeklampsi, overvægt (BMI ≥30), rygevaner og fødselsvægt >4.000 gr.
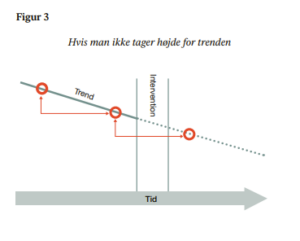
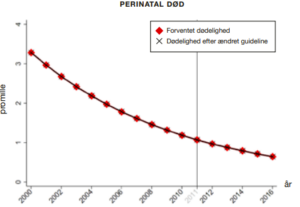
Metoden er ret afgørende i forhold til at evaluere en praksisændring. Vi har benyttet et design, der hedder Interrupted Time Series Analysis (ITSA). For de særligt sjældne udfald (dvs. død) brugte vi Poission regression. Grundtanken er, at man her tager højde for de trends, der er i forvejen. Det gør man for ikke at komme til at drage forkerte konklusioner. Lad os tage perinatal død som et eksempel. Vi har gennem de seneste 20 år her i Danmark og resten af den vestlige verden set en generelt nedadgående kurve for perinatal død. Det betyder, at hvis perinatal død opgøres to år før og to år efter, at man har indført en ny intervention (i dette tilfælde ændret igangsættelsespraksis), finder man måske, at der er sket en halvering i antallet af døde børn. Dette kunne få os til at tro, at det var interventionen, der var årsagen til reduktionen i dødsfald. Omvendt, hvis man nu foretog den samme manøvre i et lignende tidsrum, hvor der ikke havde været indført en praksisændring, er det muligt, at man ville få præcist det samme resultat. Årsagen til dette er, at når tendensen allerede er for nedadgående, vil man forvente et fald, også selv uden en intervention. Figur 3 viser en forsimplet model af dette princip. Data for perinatal død viste, at trenden allerede var nedadgående. Faktisk var den perinatale død allerede faldet med 62% i de fem år forud for interventionen. Ved at anvende ITSA-metoden tages højde for denne allerede eksisterende trend.
Resultater: Det endelige datasæt bestod af 152.887 fødsler fra perioden 2000-2016, hvor vi havde pålidelige data for de vigtigste variable, og hvor kvinden stadig var gravid ved 41+3 gestationsuger. Heraf var 213 dødfødsler (0,14%) og 262 perinatale dødsfald (0,17%). Populationen ændrede sig ikke mærkbart i og omkring denne guidelines indførelse (ex på alder og paritet).
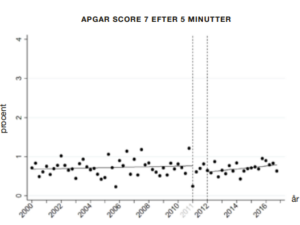
For dødfødsel, perinatal død, lav Apgar score, sectio og instrumentel forløsning viste data, at niveauet efter 2011 svarede til, hvad man ville forvente baseret på den hidtidige udvikling. Sagt på en anden måde: De ændringer, der evt. var sket for disse udfald fra før interventionen til efter, ville formentlig være sket under alle omstændigheder – intervention eller ej. Anderledes så det ud for igangsættelse, vestimulation, epiduralanalgesi og uterusruptur, hvor udviklingen efter interventionen afveg signifikant fra det forventede. Dette taler for, at praksisændringen i 2011 kan være medvirkende til ændringen i disse udfald.
Diskussion: Hovedfundene i dette studie er en manglende umiddelbar gevinst for barnet ved interventionen. Til gengæld viste data en stigning i igangsættelse, vestimulation og uterusruptur, mens sectio og instrumentel forløsning var uændret. Brugen af epiduralanalgesi steg men med en lavere hastighed end forud for den nye guideline.
Et af hovedformålene med den nye igangsættelsespraksis var at reducere antallet af intrauterine og perinatale dødsfald. Baseret på dette studie er den forventede reducerede dødelighed med tidligere igangsættelse ikke opnået. Dette skyldes måske, at der i et land som Danmark med generelt god folkesundhed og med en i forvejen meget lav perinatal dødelighed er begrænsede muligheder for at sænke den perinatale dødelighed yderligere. En større europæisk undersøgelse finder et samlet fald i intrauterin og neonatal dødelighed i alle lande og alle gestationsaldre over de sidste årtier, og betegner dette fald som ’multifaktorielt’, dvs. at mange forskellige faktorer spiller ind. Herunder er bedre prækonceptionel rådgivning, ændrede screeningsmuligheder, flere senaborter på letale misdannelser, bedre behandlingsmuligheder af syge nyfødte og fald i antal gravide, der ryger, nævnt som forklaringer (11).
Et relevant argument for de tidlige rutinemæssige igangsættelser er, at studier har fundet sammenhæng mellem stigende gestationsalder efter terminsdatoen og perinatal død (2,12). Risikoen for død er dog baseret på studier med dødsfald tilbage til 1969 og med de fleste data indsamlet mellem 1985-1996. Altså studier der ikke tager højde for de nye sundhedsmæssige landvindinger (13). Det er måske forklaringen på, at interventionen ikke har givet det forventede fald i dødelighed.
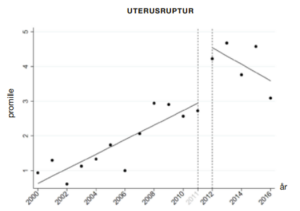
Den nye guideline har til gengæld medført en markant ændring i igangsættelsesfrekvensen fra 41% året før til 65% i året efter den nye guideline. Igangsættelse blander sig i den fysiologiske fødsel og kan på mange måder have betydning for det videre fødselsforløb i form af forlænget hospitalsophold, mindre mobilitet pga. tilslutning til drop, manglende mulighed for vandfødsel osv. (14). Yderligere øges risikoen for blandt andet hyperstimulation og uterusruptur (15,16). Vi kunne ikke i vores materiale identificere hyperstimulation, men forekomsten af uterusruptur steg markant fra 2,6 til 4,2 pr. 1.000 fødsler efter interventionen. Både igangsættelser og uterusruptur havde en relativ stigning på ca. 60% efter praksisændringen, og derefter sås et beskedent fald i sidste del af perioden. Dette er et observationelt studie, og vi kan derfor ikke vide, om der er en sammenhæng mellem flere igangsættelser og flere rupturer. Men denne sammenhæng er fysiologisk plausibel, eftersom uterusruptur er en kendt bivirkning til igangsættelser.
I Skandinavien er der generelt en meget lav risiko for intrauterin og perinatal død. Vores studie finder, at rutinemæssig igangsættelse for store grupper af lavrisiko kvinder er en ineffektiv måde at forsøge at reducere dødeligheden på og kan medvirke til unødig medikalisering af fødslen med deraf følgende bivirkninger. I kampen for at reducere dødeligheden yderligere mangler vi viden om, hvad baggrunden er, for at nogle få børn dør i den sene terminsperiode eller post term. Vi kunne ønske, at man undersøgte de bagvedliggende årsager grundigt – ikke kun medfødte misdannelser men også andre sociale mekanismer eller suboptimal svangreomsorg, der begge kan øge risikoen for død (17). Fri og lige adgang til sundhedsydelser og fokus på socioøkonomiske udfordringer ser i andre studier ud til at kunne reducere negative udfald for mødre og børn (18,19).
Referencer:
- DSOG, Wilken-Jensen C, Lassen PD, Greve T et al. Graviditet efter termin [Internet]. Vol. 2012. 2011. Available from: www.dsog.dk/files/Graviditas prolongata2011_endelig.pdf
- Gulmezoglu AM, Crowther CA, Middleton P, Heatley E. Induction of labour for improving birth outcomes for women at or beyond term. Cochrane database Syst Rev. 2012 Jun 13;6:CD004945.
- Jukic AM, Baird DD, Weinberg CR, Mcconnaughey DR, Wilcox AJ. Length of human pregnancy and contributors to its natural variation. Hum Reprod. 2013;28(10):2848–55.
- Heimstad R, Romundstad PR, Salvesen KA. Induction of labour for post-term pregnancy and risk estimates for intrauterine and perinatal death. Acta Obstet Gynecol Scand. 2008;87(2):247–9.
- Wolff SL, Lorentzen I, Kaltoft AP, Schmidt H, Jeppesen MM, Maimburg RD. Has perinatal outcome improved after introduction of a guideline in favour of routine induction and increased surveillance prior to 42 weeks of gestation?: A cross-sectional population-based registry study. Sex Reprod Healthc. 2016 Dec;10:19–24.
- Zizzo AR, Kirkegaard I, Pinborg A, Ulbjerg N. Decline in stillbirths and perinatal mortality after implementation of a more aggressive induction policy in post-date pregnancies: a nationwide register study. Acta Obstet Gynecol Scand. 2017 Jul;96(7):862–7.
- Hedegaard M, Lidegaard O, Skovlund CW, Morch LS, Hedegaard M. Reduction in stillbirths at term after new birth induction paradigm: results of a national intervention. BMJ Open. 2014 Aug 14;4(8):e005785-2014–005785.
- Danish Health Data Board. Fødselsregisteret [Danish National Birth Register] [Internet]. 2019. Available from: www.esundhed.dk/sundhedsregistre/MFR/Sider/Fødselsregisteret.aspx
- Bergholt, T, Clausen, T; Dam P. Det giver god mening at igangsætte. Politiken [Internet]. 2019 Apr 29; Available from: politiken.dk/debat/kroniken/art7151426/Det-giver-faktisk-rigtig-god-mening-at-igangsætte-fødsler
- Pedersten F. Hjælp til fødende i Danmark er verdens bedste. Berlingske Tidende [Internet]. 2017 Jun 20; Available from: www.berlingske.dk/samfund/hjaelpen-til-foedende-i-danmark-er-verdens-bedste
- Zeitlin J, Mortensen L, Cuttini M, Lack N, Nijhuis J, Haidinger G, et al. Declines in stillbirth and neonatal mortality rates in Europe between 2004 and 2010: results from the Euro-Peristat project. J Epidemiol Community Health. 2016 Jun;70(6):609–15.
- Heimstad R, Skogvoll E, Mattsson LA, Johansen OJ, Eik-Nes SH, Salvesen KA. Induction of labor or serial antenatal fetal monitoring in postterm pregnancy: a randomized controlled trial. Obstet Gynecol. 2007 Mar;109(3):609–17.
- Weiss E, Krombholz K, Eichner M. Fetal mortality at and beyond term in singleton pregnancies in Baden-Wuerttemberg/Germany 2004-2009. Arch Gynecol Obstet. 2014 Jan;289(1):79–84.
- Simpson KR, Thorman KE. Obstetric “conveniences”: elective induction of labor, cesarean birth on demand, and other potentially unnecessary interventions. J Perinat Neonatal Nurs. 2005;19(2):134–44.
- Azanta D. SPC Angusta. 2019;1–9. Available from: mri.cts-mrp.eu/Human/Downloads/DK_H_2584_001_FinalSPC.pdf
- Rydahl E, Eriksen L, Juhl M. Effects of induction of labor prior to post-term in low-risk pregnancies: a systematic review. JBI database Syst Rev Implement reports. 2019 Feb;17(2):170–208.
- Brown HL, Smith M, Beasley Y, Conard T, Musselman AL, Caine VA. Infant Mortality Lessons Learned from a Fetal and Infant Mortality Review Program. Matern Child Health J. 2017 Dec;21(Suppl 1):107–13.
- Flenady V, Wojcieszek AM, Middleton P, Ellwood D, Erwich JJ, Coory M, et al. Stillbirths: recall to action in high-income countries. Lancet (London, England). 2016 Feb 13;387(10019):691–702.
- Villadsen SF, Mortensen LH, Andersen AMN. Ethnic disparity in stillbirth and infant mortality in Denmark 1981-2003. J Epidemiol Community Health. 2009 Feb;63(2):106–12.